遺伝子改変T細胞療法
はじめに
遺伝子改変T細胞とは、がん細胞の抗原提示装置に結合しているがん抗原を認識するT細胞受容体(TCR)、あるいは、がん細胞を認識する抗体の標的抗原認識部分とリンパ球活性化分子との融合蛋白(Chimeric antigen receptor:CAR)遺伝子を、Tリンパ球に導入し強制発現させ、高いがん抗原への特異性を持たせた人工リンパ球です。前者はTCR遺伝子改変T細胞(TCR-T)、後者はキメラ抗体受容体遺伝子改変T細胞(CAR-T)と呼ばれています。本項では、最近わが国でも承認をされたCAR-Tを中心に解説します(下図)。
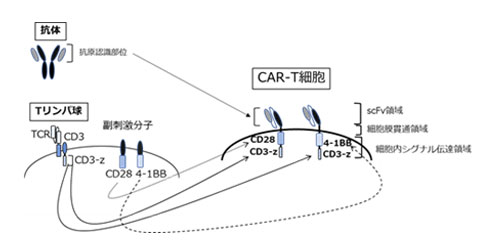
遺伝子改変T細胞の製造方法
遺伝子改変T細胞は、患者由来のTリンパ球にTCRやCARの遺伝子を導入して作られます。その工程は、1)患者さんの末梢血のリンパ球を採取し、2)ウイルス由来のベクターを用いてTCR遺伝子やCAR遺伝子をT細胞に導入し、3)遺伝子導入された細胞を増殖し、4)増殖した細胞製剤に病原微生物や有害物質が含まれていないかを品質管理を行い、5)患者さんに投与するとなります。この工程は、TCR-T、CAR-Tとも同じです。現時点では、患者さん自身のリンパ球を用いて遺伝子改変T細胞を作るため、患者さん毎に上記のすべての工程が必要となり、治療を始めるまでに時間要すると同時に高額な費用が必要となります(下図)。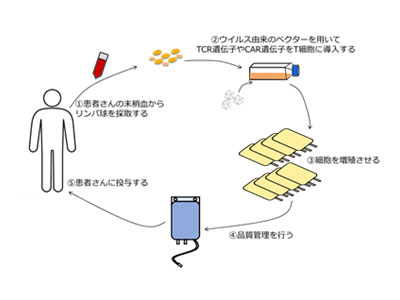
CAR-T細胞
CAR-T細胞は、「抗体由来の標的認識部位とリンパ球活性化分子の融合蛋白」を強制発現した、高い抗原特異性と強い抗腫瘍活性を持つ人工リンパ球です。最初に臨床開発が行われ、わが国を含む複数の国で既に承認されているのが、Bリンパ球が持つCD19を標的としたCAR-T細胞です。承認に至った臨床試験の結果を簡単にまとめると、以下のようになります。
再発又は-難治性の小児並びに成人CD19陽性Bリンパ芽球性白血病を対象とした国際多施設共同第Ⅱ相試験(ELIANA試験)では、中間解析時点で全寛解率は82%であると共に、長期間の寛解が得られたことが報告されています(文献1)。
再発又は-難治性のCD19陽性成人びまん性大細胞性B細胞リンパ腫(DLBCL)を対象とした国際多施設共同第Ⅱ相試験(JULIET試験)でも、中間解析時点で、58.8%の奏功率(完全寛解率+部分寛解率)が得られるとともに、その効果が長期間得られたことが報告されています(文献2)。
副作用に関しては、強力なリンパ球の活性化に伴うサイトカイン放出症候群が約60%の患者で認められたほか、低ガンマグロブリン血漿(ガンマグロブリンを作る細胞の元となるCD19陽性の正常B細胞が障害を受けた結果)、発熱、低血圧等が見られていますが、対応方法のマニュアルに沿った治療を行うことで管理可能であったと報告されています。これらの治験結果を踏まえ、2019年3月に、CD19に対するCAR-T(Novartis社、商品名キムリア)が承認されました。
そのほかのCAR-Tとして、CD19と同様のBリンパ性の造血器腫瘍を標的としたCD20に対するCAR-Tのほか、固形腫瘍を標的にした数々のCAR-T細胞の開発が精力的に行われています。
TCR遺伝子改変T細胞
CAR-Tの影に隠れていますが、TCR-Tの開発も進められています。我が国においても、NY-ESO-1をはじめとするがん関連抗原に特異的なTCR遺伝子改変T細胞の治験が進められており、有望な結果も報告されています。CD19 CAR-Tに代表される血液腫瘍を狙ったCAR-Tとは異なり、固形がんに対する臨床開発が先行しており、その成果に期待が集まっています。
遺伝子改変T治療は高額である
最近承認された、CD19に対するCAR-T(キムリア)の1患者あたりの薬価は3349万3407円です。再発または難治性CD19陽性のB細胞性急性リンパ芽球性白血病(B-ALL)、再発または難治性びまん性大細胞型B細胞リンパ腫(DLBCL)が対象となり、推定投与患者数がピーク時で216名と限定されていることから、その保険財政に与える影響は限られています。一方、今後研究が進み、様々な遺伝子改変T細胞を用いた治療が承認されれば、その保険財政に与える影響は無視できなくなります。
現在、遺伝子導入にウイルスを用いない方法や、複数の患者さん用にあらかじめ準備した他人のリンパ球由来の遺伝子改変細胞の開発が進められており、将来的に身近な治療になることが期待されています。
【参考文献】
1. Mueller KT, et al. Clin Cancer Res. 2018;24:6175-6184.
2. Schuster SJ, et al. N Engl J Med. 2019; 380:45-56.



